
Compartilhar
Responder Questão:
Pesquisadores de Harvard desenvolveram uma técnica para preparar nanoestruturas auto-organizadas na forma que lembram flores. Para criar as estruturas de flores, o pesquisador dissolveu cloreto de bário e silicato de sódio num bequer. O dióxido de carbono do ar se dissolve naturalmente na água, desencadeando uma reação que precipita cristais de carbonato de bário. Como subproduto, ela também reduz o pH da solução que rodeia imediatamente os cristais, que então desencadeia uma reação com o silicato de sódio dissolvido. Esta segunda reação adiciona uma camada de sílica porosa que permite a formação de cristais de carbonato de bário para continuar o crescimento da estrutura.
(“Beautiful "flowers" self-assemble in a beaker”. Disponível em <https://www.seas.harvard.edu/news/2013/05/beautiful-flowers-self-assemblebeaker>. Acesso em 10 ago. 2013)
Na tabela ao lado são mostrados valores de produto de solubilidade de alguns carbonatos.
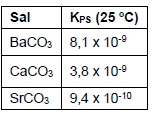
a) Suponha que num bequer foram dissolvidos cloretos de bário, cálcio e estrôncio de modo que as concentrações de cada sal é igual a 1umol.L-1. Com a dissolução natural do gás carbônico do ar, qual carbonato irá primeiramente cristalizar?
b) Num bequer há uma solução 1umol.L-1 de cloreto de bário. Calcule qual a concentração de íons carbonato necessárias para que o cristal de carbonato de bário comece a se formar.
TEMPO NA QUESTÃO
 00:00:00
00:00:00
 Meu Desempenho
Meu Desempenho
Química Geral
Total de Questões: ?
Respondidas: ? (0,00%)
Certas: ? (0,00%)
Erradas: ? (0,00%)
Somente usuários cadastrados!


 Estatísica da Questão
Estatísica da Questão
 Alternativa mais respondida
Alternativa mais respondida
 Comentário dos estudantes
Comentário dos estudantes